







Kalliopi-Anna Poulia
Dr, MSc, PhD
Clinical Nutritionist-Dietitian
Laiko General Hospital of Athens, Greece
lpoulia@gmail.com
10.0 Manejo dietético en hemodiálisis en el hogar
Objetivos de aprendizaje
- Entender la importancia de la nutrición en pacientes sometidos a HHD
- Para identificar las necesidades nutricionales de un paciente con ERC estadio 5
- Identificar las diferencias entre las necesidades nutricionales de un paciente con HHD más frecuente en comparación con la hemodiálisis convencional
- Identificar cómo los problemas nutricionales comunes pueden ser manejados en pacientes sometidos a HHD
Introducción
La intervención dietética es de gran importancia para los pacientes con enfermedad renal crónica (ERC), tanto para el resultado de la enfermedad como para la prevención o el tratamiento de la desnutrición (sobrenutrición y desnutrición), que es bastante común en pacientes con ERC. Desnutrición es un término general que indica un estado de nutrición en el que una deficiencia o exceso (o desequilibrio) de energía, proteínas y otros nutrientes causa efectos adversos mensurables en la forma del tejido/cuerpo (forma, tamaño y composición) y función, y resultado clínico1. El primero y más importante es la Desnutrición Proteico-Energética (PEM) o la Pérdida de Energía Proteica (PEW), que se define como la falta de suficiente energía o proteína para satisfacer las demandas metabólicas del cuerpo2. Las causas de la desnutrición son:
- Una ingesta inadecuada de alimentos secundaria a anorexia causada por uremia y alteración de la sensación gustativa.
- Mayores demandas debido a enfermedades o enfermedades agudas.
- Capacidad deficiente para preparar comida.
- Dietas prescritas desagradables (baja en sal, restricción de líquidos, baja en potasio, baja en fósforo).
- El propio procedimiento de diálisis debido a la pérdida de nutrientes (péptidos proteínicos, vitaminas solubles en agua, etc.).
- Hipermetabolismo debido a la inflamación crónica.
- Trastornos endocrinos por uremia3,4.
Por lo tanto, una evaluación nutricional detallada es de suma importancia para proporcionar una atención óptima a las personas con ERC en todas las etapas de la enfermedad. Clásicamente, se utilizan tres líneas principales de investigación, es decir, las medidas bioquímicas, la ingesta dietética y la composición corporal para evaluar el estado nutricional de la proteína y la energía.
La ingesta de proteínas es de gran importancia, ya que durante la HD se produce pérdida de proteínas. Se debe incluir una ingesta suficiente de proteínas de alto valor biológico. Al mismo tiempo, el control de fosfato requiere el uso correcto de aglutinantes de fosfato. Además, la restricción de sodio es necesaria para controlar la sed y la ingesta de líquidos y facilitar un mejor control de la presión arterial. Finalmente, el control del potasio es de gran importancia, y se logra principalmente por la restricción de la ingesta de alimentos ricos en potasio, principalmente de los grupos de frutas y verduras.
El manejo dietético de los pacientes sometidos a hemodiálisis domiciliaria (HHD) depende del tipo de hemodiálisis que siguen los pacientes. Para los pacientes que siguen un programa de HHD tres veces cuatro horas por semana, las restricciones dietéticas siguen siendo las mismas que las HD convencionales. Al aumentar la frecuencia y la duración de la hemodiálisis en el hogar (Hemodiálisis Diaria Corta (SDHD) o Hemodiálisis Nocturna (NHD)) aumentamos la cantidad de productos de desecho eliminados del cuerpo de los pacientes. Por lo tanto, la mayoría de las restricciones existentes para la HD convencional se pueden reducir.
10.1 Control bioquímico con hemodiálisis más frecuente
Debido a la alta prevalencia de malnutrición después del inicio de la HD, una medición de referencia es útil para controlar el estado nutricional. Al comienzo de la HHD, el estado nutricional ya puede estar influido negativamente por las restricciones dietéticas de la HD convencional o incluso por el cumplimiento en los planes dietéticos restrictivos en etapas más tempranas de la ERC.
La pérdida de peso involuntaria, que alcanza el 5% del peso corporal en 3 meses, se considera una pérdida de peso significativa y debe ser una alerta de acción para prevenir la desnutrición. Además, los niveles de apetito, de fósforo, de colesterol y de albúmina limitados deben detectarse temprano y se debe alentar a los pacientes a aumentar su consumo de energía y proteínas.
De acuerdo con los datos de investigación disponibles, después de unas pocas semanas del inicio de la hemodiálisis domiciliaria frecuente (FHHD) aumenta el apetito y la ingesta de alimentos también mejora, lo que resulta en el aumento de los niveles de albúmina y una mejora del estado nutricional5,8. No obstante, el estado nutricional debe vigilarse de cerca en los pacientes sometidos, ya que la detección temprana de alteraciones en el estado nutricional es importante para el tratamiento precoz de la malnutrición de acuerdo con la Tabla 10.1.
Las pautas pueden variar un poco y cada unidad elegirá qué pautas seguir. De acuerdo con las directrices de KDOQI para la albúmina sérica CK Care9 <4 g/dl, prealbúmina <30 mg/dl, creatinina prediálisis<10 mg/dl y colesterol <150 mg/dl son marcadores clínicamente útiles que indican una alta posibilidad de desnutrición proteico-energética en pacientes con ERC, mientras que la Society of Renal Nutrition and Metabolism recientemente incluyó albúmina sérica <3.8 g/dl como uno de tres criterios diagnósticos bioquímicos para la pérdida de energía proteica (entre los niveles de transtiretina y colesterol)10. Además, de acuerdo con la Guía EBPG sobre Nutrición11, el IMC debería ser> 23 kg/m2 en pacientes en hemodiálisis de mantenimiento. Estos parámetros deben controlarse regularmente para evaluar los resultados nutricionales y las necesidades de los pacientes.
Tabla 10.1: Sugiere estrategias para monitorizar el estado nutricional y guia terapéutica en ERC avanzada12
| Evaluación (mensual) simple | Resultados | Posibles intervenciones |
| Peso/Peso Ideal Albúmina sérica Creatinina sérica |
Descenso continuo o <85% IBW <4.0 g/dl Valores relatives bajos pre-diálisis |
Sospechar PEW y examen detallado Consejo nutricional Considerar medidas preventivas |
| Evaluación temprana detallada | Resultados | Posibles intervenciones (simple) |
| Prealbúmina sérica Transferrina sérica Masa corporal magra y/o masa adiposa SGA |
<30mg/dl y/o <200mg/dl y/o Reducción inesperada Deterioro |
Consejo Dietético: ingesta proteica 1.2g/kg/d, Ingesta calórica 30-35 Kcal/día Aumentar la dosis de dialysis a Kt/V>1.4 Utilizar membranas biocompatibles Estimular la motilidad Gl superior |
| Repetir la evaluación detallada (2-3 meses después de la anterior) | Resultados | Posibles intervenciones (más complejas) |
| Prealbúmina sérica Transferrina sérica Masa corporal magra y/o masa adiposa Proteina C-reactiva |
<30mg/dl y/o <200mg/dl y/o Reducción inesperada >10 mg/l |
Apoyo nutricional (Nutrición oral suplementos, nutrición enteral, IDPN si es necesario) Factores anabólicos Estimulantes del apetito (experimental) Antiinflamatorios (experimental) |
10.2 Ingesta nutricional: menos acumulación implica más libertad dietetica
Debido a la frecuencia creciente de la diálisis, la FHHD puede proporcionar una función más «fisiológica» para los pacientes, permitiéndoles excretar los productos de desecho del metabolismo de forma más eficiente. En consecuencia, las restricciones aplicadas a los pacientes que se encuentran en HD convencional (principalmente para el control de electrolitos, como el fosfato y el potasio, y la restricción en el control de líquidos) pueden reducirse, en función de los resultados de los análisis del paciente. Los pacientes en FHHD de la cohorte KIHDNEy mostraron recientemente parámetros estables en los desórdenes minerals y de los huesos con pocas restricciones dietéticas, muchos pacientes estaban en el rango deseado de fosfato y presentaban una mejora significativa en los niveles de bicarbonato en comparación con su estado basal24.
La ingesta nutricional se puede medir en calorías para la energía o en gramos para las proteínas, usualmente expresadas por kilogramo de peso corporal por día (kcal/kg/día o g/kg/día)
10.2.1 Consumo de energía
Una ingesta energética suficiente es esencial para lograr un balance de nitrógeno positivo. Un consumo de energía de 35 kcal/kg/día se asocia con un mejor balance de nitrógeno y es recomendable en pacientes con ERC estable en el rango de peso corporal ideal ± 10%13. El consumo de energía recomendado en un paciente en HD crónica clínicamente estable es de 30-40 kcal/kg/día, ajustado a la edad, el sexo y la mejor estimación del nivel de actividad física. Para pacientes mayores de 60 años u obesos, la prescripción de ingesta de energía no debe exceder las 30 kcal/kg/día9,11,14.
Los pacientes con sobrepeso o desnutridos pueden necesitar ajustes en el suministro de energía para garantizar una mejor cobertura de sus necesidades. La ingesta de energía para pacientes mayores de 60 años debe ser de 30 kcal/kg/día debido a sus necesidades energéticas reducidas si tienen una vida más sedentaria debido a la edad. Sin embargo, se debe promover la actividad física regular ya que ayuda a mantener la funcionalidad de los músculos y mejora la resistencia y la salud cardiovascular.
10.2.2 Ingesta de proteínas
Las necesidades proteícas de los pacientes en mantenimiento HD superan las necesidades de las personas sanas normales ya que el tratamiento de diálisis en sí mismo induce pérdidas significativas de nutrientes, particularmente aminoácidos, oligopéptidos, vitaminas solubles en agua y oligoelementos. Además, el procedimiento de diálisis es catabólico, iinduce estrés catabólico y liberación de citocinas proinflamatorias, que aumentan las necesidades de proteínas15.
De acuerdo con las pautas disponibles;
- La ingesta de proteína recomendada es de 1.0-1.5 g/kg/día en pacientes en hemodiálisis crónica clínicamente establess y nPNA de al menos 1.0 g/peso corporal/día.
- La ingesta proteica óptima para un paciente de diálisis en mantenimiento que está gravemente enfermo es de al menos 1,2 a 1,3 g/kg/día4,11.
- Más específicamente, para pacientes con HHD, los requisitos de proteínas son de gran importancia ya que el aumento de la frecuencia de la diálisis aumenta las pérdidas de proteínas.
Por lo tanto, el nivel más alto de recomendaciones debe aplicarse a los pacientes sometidos a FHHD. En general, se ha informado que la ingesta de proteínas aumenta después del aumento de la frecuencia de diálisis, con el consiguiente aumento de la ingesta de fosfato, sin alterar los niveles sanguíneos de fosfato, incluso con una potencial reducción del uso de quelantes de fósforo16. No obstante, la ingesta de proteínas es de gran importancia y debe vigilarse de cerca para garantizar una cobertura suficiente de las necesidades de los pacientes.
La ingesta de proteína debe ser de alto valor biológico, es decir, de orígen animal, p.ej aves de corral, carne, claras de huevo, soja, queso crema, etc. En FHHD proteína animal con alto contenido en fósforo (pescado pequeño, productos lácteos, queso, carne cercana a los huesos) por lo general puede consumirse más libremente, en comparación con HD convencional, porque los productos de desecho del metabolismo proteico se excretan más eficientemente. En el caso de deficiente control de fosfatos, se debe limitar el consumo de alimentos con alto contenido de fosfato, y la ingesta de proteína solo en las comidas en las que el paciente que esté tomando aglutinantes de fósforo, para reducir directamente la absorción intestinal de fósforo.
Si se informa de alteración en el sabor de la proteína animal (sabor metálico), se han de proporcionar fuentes alternativas de proteína de alto valor biológico. El enriquecimiento de los alimentos con suplementos de proteínas podría ser una forma de aumentar la dosis de proteínas.
10.2.3 Consumo de grasa
La ERC aumenta el riesgo de desarrollar enfermedades cardiovasculares17, debido a la inflamación, la proporción alterada de calico/fósforo y factores de riesgo preexistentes como la diabetes mellitus. Por lo tanto, se deben tener en cuenta todos los factores de riesgo cardiovascular relacionados con la nutrición18,19. En pacientes en HD, se debe poner énfasis en la calidad del consumo de grasas;
- La grasa saturada debe limitarse a <10% de la ingesta total de energía.
- Colesterol <250 mg/día.
- Ácidos Monoinsaturados deben ser el 10-20% de la ingesta total de energía (TEE).
- La grasa poliinsaturada debe proporcionar alrededor del 10% de TEE.
Por lo tanto, las fuentes de grasas saturadas, como productos lácteos enteros, queso, carne grasosa, aves con piel, alimentos fritos, mantequilla y crema grasas deben evitarse, mientras que la ingesta de aceite de oliva debe ser una de las principales fuentes de grasa. Se debe hacer hincapié en la ingesta de ácidos grasos ω-3, que podrían formar parte del plan dietético en pacientes sometidos a HHD con mayor frecuencia o duración, debido a un mejor control de los niveles de fosfato. La ingesta de pescado graso, como el bacalao o el salmón, podría incluirse al menos una vez a la semana, con el uso correcto de aglutinantes de fosfato en pacientes con escaso control de fosfato.
10.2.4 Vitaminas y oligoelementos
Los pacientes en diálisis son propensos a desarrollar deficiencias vitamínicas debido a un metabolismo renal anormal, una ingesta dietética inadecuada y el cumplimiento de estrictas restricciones dietéticas, pérdida de la absorción gastrointestinal y pérdidas en diálisis. Las pérdidas dependen del tipo de diálisis y su duración, ya que la diálisis de alto flujo y alta eficiencia atenúa las pérdidas en vitaminas solubles en agua. Las deficiencias de vitaminas se desarrollan lentamente, pero pueden afectar la calidad de vida de los pacientes. Debe evaluarse el estado vitamínico de cada paciente de forma individual, de acuerdo con la edad, el sexo, la ingesta dietética, las pérdidas de diálisis, la función renal residual y el tipo de diálisis antes de suscribirse a una terapia vitamínica complementaria11. Los niveles de vitaminas en sangre, junto con la detección temprana de los síntomas de deficiencias vitamínicas, son importantes para asegurar la individualización del tratamiento.
10.2.4.1 Vitaminas solubles en agua
Durante la hemodiálisis, se pierde una cantidad significativa de vitaminas en el dializado. En HD convencional, debido a las restricciones dietéticas de potasio en vegetales y frutas, los pacientes son particularmente propensos a deficiencias en ácido fólico y vitamina C. Se necesita ingesta de ácido fólico (1 mg-5 mg) para la prevención de hiperhomocisteinemia. La vitamina C también se debe tomar como un suplemento (75-90 mg), aunque esto es más importante en aquellos que restringen sus verduras y frutas11.
La deficiencia de tiamina es común en pacientes en hemodiálisis ya que se elimina fácilmente por la HD y, al mismo tiempo, la ingesta dietética a menudo es inadecuada. Las fuentes dietéticas de tiamina incluyen semillas, legumbres y carne de cerdo. El beriberi es la condición más conocida causada por la deficiencia de tiamina, mientras que otras manifestaciones incluyen síntomas neurológicos (encefalitis de Wernicke). Actualmente, todos los suplementos vitamínicos para pacientes renales incluyen tiamina11.
La deficiencia de Rivoflabina no es común, a pesar de que está bien aclarada durante una sesión de hemodiálisis, ya que sus principales fuentes incluyen carne magra, huevos, cereales y pan y alimentos incluidos en la dieta de los pacientes con ERC en etapa final. Las necesidades de B6 pueden ser elevadas por la eritropoyesis acelerada mediante el uso de eritropoyetina. La B12 es necesaria para la prevención de la anemia perniciosa y para un metabolismo óptimo del ácido fólico. Se encuentra en cantidades suficientes en la carne, la leche y la yema de huevo, mientras que el uso suplementario es seguro en la ingesta de pacientes renales es generalmente cerca de DRI11.
Las recomendaciones para la ingesta de vitaminas y suplementos para pacientes en hemodiálisis se resumen en la tabla 10.2. No hay recomendaciones específicas para los pacientes sometidos a FHHD y se necesita más investigación para identificar las diferencias en las necesidades vitamínicas para los pacientes con HD en diferentes tipos y frecuencia de tratamiento.
10.2.4.2 Vitaminas liposolubles
Las vitaminas liposolubles deben tratarse con precaución, ya que se almacenan en el cuerpo y el riesgo de toxicidad es mayor. Las deficiencias de vitamina A son raras en pacientes renales ya que no se eliminan por hemodiálisis. Por lo tanto, el peligro de toxicidad es mayor y no se recomienda el uso de suplementos. Las necesidades diarias pueden cubrirse con fuentes dietéticas que incluyen productos lácteos, aceite de pescado y zanahorias. Con respecto a la vitamina K, no hay evidencia de deficiencias en pacientes con ERC que reciben suficiente ingesta con la dieta11.
Tabla 10.2. Ingesta dietética recomendada y suplementos de vitaminas11
| Vitaminas | Recomendaciones diarias |
|---|---|
| Vitaminas solubles en agua | |
| Tiamina (B1) | 1.1-1.2 suplemento |
| Riboflavina (B2) | 1.1-1.3 suplemento |
| Niacina (B3) | 14-16mg suplemento |
| Ácido Pantotenico (B5) | 5 mg suplemento |
| Piridoxina (B6) | 10 mg suplemento |
| Biotina (B8) | 30 μg suplemento |
| Ácido Fólico (B9) | 1-5 mg suplemento |
| Cobalamina (B12) | 2.4 mg suplemento |
| Vitamina C | 75-90 mg suplemento |
| Vitaminas Liposolubles | |
| Vitamina A | 700-900 μg ingesta – no suplemento |
| Vitamina K | 90-120 μg - no suplemento |
| Vitamina E | 400-800 IU suplemento para CVD secundario, prevención y calambres |
10.2.5 Electrolitos y minerales
10.2.5.1 Sodio y fluidos
La restricción de sodio está indicada para todas las etapas de la ERC ya que es esencial para el control del volumen extracelular y para un mejor control de la presión arterial. En HD, el control del sodio es aún más importante, ya que facilita el cumplimiento de las restricciones de líquidos y previene el aumento de peso interdiálisis en pacientes anúricos y oligúricos, dado que reduce la sed. En pacientes en Hd deben evitarse los sustitutos de sal que contienen cloruro de. La sal puede ser sustituida por el uso de hierbas y especias. Más específicamente, el sodio debe restringirse a no más de 80-100 mmol (2000-3000 mg) o 5-6 g (75 mg/kg/día).
La ingesta de líquidos generalmente es más generosa en pacientes que usan FHHD en el hogar porque se extraen más líquido durante la semana.
Por lo tanto, muchos pacientes pueden superar el límite de 500-1000 ml además de la producción diaria de orina. No existen recomendaciones estrictas para la ingesta de líquidos en pacientes con FHHD, pero el objetivo es controlar la ganancia de peso interdiálisis11.
En los casos de pacientes a los que les resulta difícil controlar su ingesta de líquidos, todos los alimentos que son líquidos a temperatura ambiente (18-20°) se deben contar como líquidos, excepto los aceites. El control de la sed puede se puede facilitar reduciendo la ingesta de sal,con el consumo de líquidos refrigerados, de cubitos de hielo en lugar de agua, la adición de limón al agua y el uso de chiclets para hidratar la boca20,21.
10.2.5.2 Potasio
En sujetos sanos, el 90% del potasio en la dieta se excreta por los riñones. Para los pacientes en diálisis que limitan la ingesta dietética y una diálisis adecuada, pueden alcanzar niveles de potasio aceptables. El potasio existe en casi todos los alimentos, por lo que se deben limitar las restricciones severas, a fin de garantizar un equilibrio en la dieta y la calidad de vida de los pacientes.
En la mayoría de los pacientes que reciben HHD de frecuencia aumentada, los niveles de potasio se mantienen más fácilmente dentro de los niveles normales. Por lo tanto, la dieta puede ser más libre, en términos de consumo de frutas y verduras. El consumo de fibra también es más fácil de mantener dentro de las cantidades recomendadas, lo que facilita la prevención del estreñimiento. En pacientes con ERC, la excreción intestinal de potasio se incrementa como un mecanismo compensatorio y la prevención del estreñimiento también contribuye a la prevención de la hipercalemia.
La hipercalemia causa náuseas, debilidad, entumecimiento u hormigueo, pulso lento, ritmo cardíaco irregular y un alto riesgo de insuficiencia cardíaca o muerte súbita. Después de cualquiera de estos signos, hay que medir los niveles séricos de potasio y documentarse antes de HD. En pacientes con potasio prediálisis> 6 mmol/l, la ingesta diaria de potasio no debe superar los 50-70 mmol (1950-2730 mg) o 1 mmol/kg/día11. Si los niveles de potasio son elevados repetidamente, se debe recomendar a los pacientes que reduzcan su consumo de potasio, evitando las frutas y verduras ricas en potasio (plátanos, naranjas, patatas, tomates, etc.) y eligiendo alimentos con niveles bajos de potasio (manzanas, peras, lechugas, zanahorias, vegetales hervidos, frutas peladas o hervidas y picadas).
Tabla 10.3. Pasos para calcular la prescripción inicial de quelantes22
| Paso | Ejemplo | Ejemplo |
|---|---|---|
| Ingesta de Fosfato | Total de P ingerido en la dieta | 1000 al día o 7000/semana |
| Cantidad absorbida (50-70% de una dieta variada sin ERC) (53% ERC vs 77% no renal) |
Ingerido en la dieta multiplicado por 50-60% absorbido | 600 al día or 4200/semana |
| Cociente de aclaramiento HD/PD HD = 800 por tratamiento PD=300-315 al día |
Cociente de abs - aclaramiento = P remante para ser removido por el quelante de fósforo | HD: 4200-2400 = 1800 mg P/wk or 257 mg/día PD: 4200-2205 = 1995 mg P/wk or 285 mg/día |
| Dividir entre el poder de absorción estimado del quelante de elección | P remanente/poder de absorción 257/39 (aprox. P absorción para 1g CaCO3) = 6.5 g CaCo3 | 257/45 (aprox. P absorción para 1g acetato de calcio)= 5.7 g 257/15-30 (aprox. P absorción para 1 AI(OH)3 tableta = 12-17 tabletas 257/64 (aprox. P absorción o 800mg sevelamer HCI) = 4 tabletas 257/32 (approx. P absorción para 400mg sevelamer HCL) = 8 tabletas Nota: Los calculus para OD deben usar 285 en lugar de 257 |
Nota: La tabla anterior estima la prescripción inicial basada en la absorción media de fósforo, el aclaramiento medio de la dialysis y el potencial aproximado de absorción del quelante de elección. La dosis debe ser monitorizada y ajustada basándose en la respuesta individual del paciente.
10.2.5.3 Fosfato
La hiperfosfatemia está relacionada con hiperparatiroidismo, calcificación y enfermedades óseas minerales. Por lo tanto, se debe vigilar de cerca el fosfato sérico. En pacientes sometidos a HD, las altas necesidades de proteínas pueden conducir a la acumulación de fósforo, ya que cada sesión de HD solo elimina 500-700 mg de fosfato. Los alimentos con proteínas proporcionan 12-16 mg de fosfato/g, mientras que los productos lácteos tienen el contenido más alto11. La selección de alimentos proteínicos con el menor contenido de fósforo puede ayudar a lograr los objetivos de fosfato, sin afectar la ingesta de proteínas.
A medida que aumenta la frecuencia de HD, los niveles de fosfato se pueden mantener dentro de los niveles normales más fácilmente, y por lo tanto, los pacientes pueden seguir un plan dietético más libre. En pacientes que no alcanzan sus objetivos de niveles de fosfato, el uso apropiado de los quelantes de fósforo (tipo, dosis y tiempo) aumentará la excreción de fósforo. En la tabla 10.3, se describen los pasos para calcular la prescripción inicial de aglutinante para HD convencional y en la tabla 10.4 se enumeran los principales compuestos de unión a fosfato. Es importante que el control del fosfato no comprometa la ingesta de proteínas. De acuerdo con las directrices nutricionales existentes, se recomienda la ingesta de 800-1000 mg o <17 mg/kg/día de fosfato4,11.
La hemodiálisis domiciliaria nocturna (NHHD) elimina aproximadamente 5638 mg de fósforo por semana, lo que se atribuye a la mayor frecuencia y a la larga duración de la diálisis. Este hecho libera la dieta de los pacientes que pueden controlar sus niveles de fosfato con un uso mínimo o nulo de los quelantes de fosfato. La hemodiálisis diaria a corto plazo (SDHD) elimina un poco más de fosfato que la HD convencional; sin embargo, el apetito mejorado que se observa en los pacientes con SDHD y el consiguiente aumento de la ingesta de proteínas y fósforo generalmente dejan a los pacientes con un balance neto de fosfato positivo neto23. En caso de hiperfosfatemia, se debe considerar el uso de aglutinantes de fosfato.
En la Tabla 10.4 se presentan los principales compuestos de unión a fosfato.
Tabla 10.4. Compuestos de unión a fosfato22
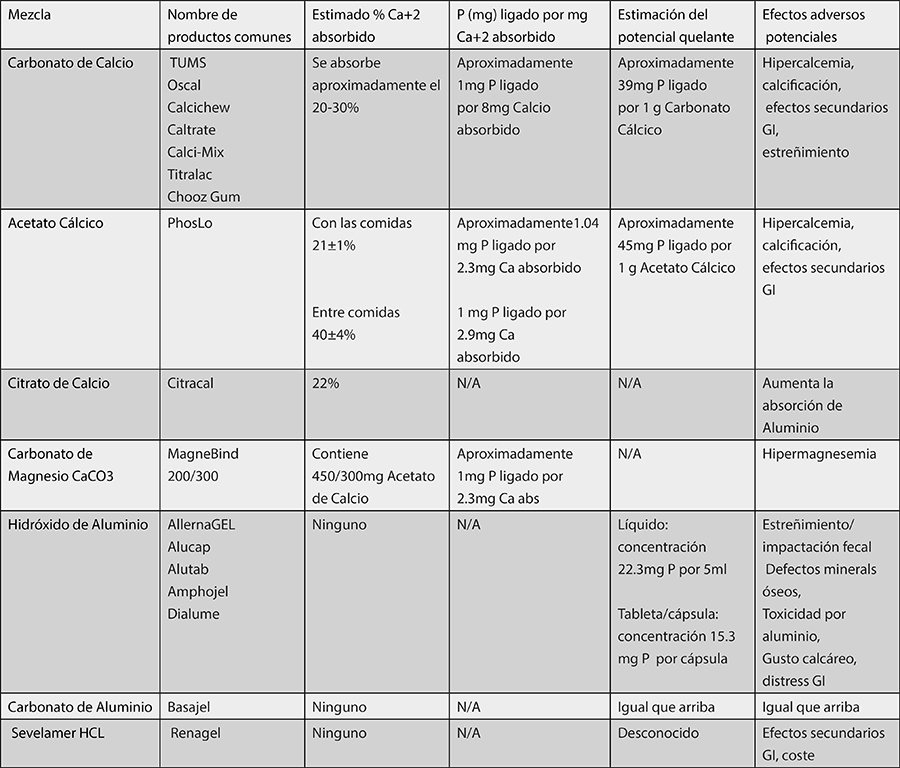
Resumen
La nutrición es muy importante para las personas con FHHD aunque más diálisis significa menos restricciones. El potasio, el fosfato, el líquido, las proteínas y las vitaminas son elementos importantes. Cada paciente debe recibir información personalizada según sus necesidades diarias, preferencias alimenticias y resultados analíticos.
Actividad de aprendizaje
- ¿Cuáles son las principales causas de desnutrición en pacientes con ERC?
- ¿Qué marcadores biológicos se deben monitorizar para la detección temprana de desnutrición en hemodiálisis?
- ¿Cuáles son las necesidades de energía de los pacientes sometidos a HD?
- ¿Cuáles son las necesidades de proteínas para los pacientes que reciben HHD con frecuencia?
- Describa 5 diferencias en la dieta de un paciente cuando pasa de hemodiálisis domiciliaria convencional a frecuente.
EDTNA/ERCA Secretaría
Correo: secretariat@edtnaerca.org



